Esta sección es una adaptación del trabajo: “DICER1: mutations, microRNAs and mechanisms” (DICER1: mutaciones, micro RNA y mecanismos), publicado en Nature Reviews Cancer por Foulkes, Priest y Duchaine (PMID 25176334). Para obtener más información, consulte el artículo original
Funciones moleculares
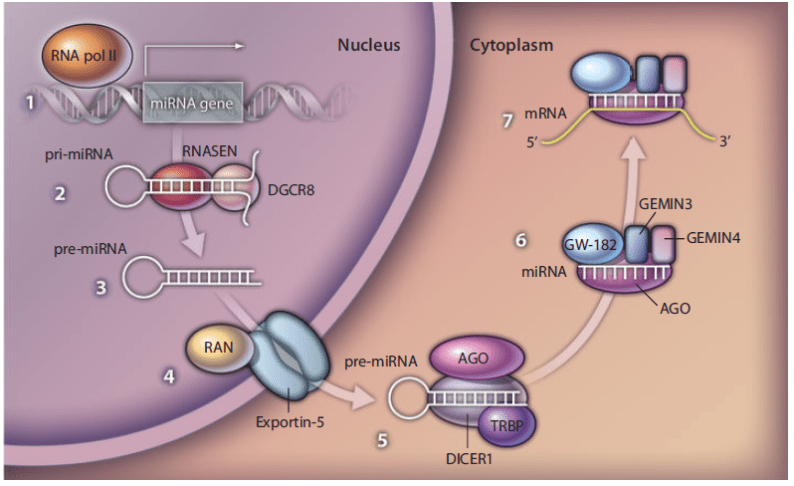
La proteína Dicer es un endoribonucleasa responsable de la producción de micro RNA maduros (miRNA), que son moléculas de RNA de cadena sencilla que tienen como objetivo a un RNA mensajero (mRNA) y poseen un rol importante en la regulación de la expresión génica al reprimir la síntesis de proteínas. La forma humana de la proteína Dicer se denomina DICER1, codificada por el gen DICER1 y se expresa extensamente en varios tejidos. DICER1 participa en la vía de silenciamiento génico mediada por miRNA, donde un miRNA se hibrida de manera imperfecta para abordar los mRNA. A su vez, esto generalmente lleva a una represión de la traducción del mRNA y la iniciación de la degradación del mRNA. Se produce una transcripción del miRNA primario (pri-miRNA) a través de una transcripción de un gen miRNA por la enzima RNA polimerasa II. El pri-miRNA luego es procesado en el núcleo por DROSHA (también conocido como RNASEN), un RNA endonucleasa y la proteína de unión a RNA DGCR8 (también conocido como PASHA), lo cual resulta en la producción de una horquilla de RNA que contiene el miRNA. Esta horquilla de miRNA prematuro (pre-miRNA) se exporta luego al citoplasma a través de los poros nucleares. La proteína DICER1 citoplásmica adhiere la pre-miRNA para liberar el miRNA corto maduro (~21 nucleótidos). Este miRNA luego se carga en una proteína Argonauta (AGO) que forma el núcleo del complejo de silenciamiento inducido por miRNA (miRISC). El miRISC luego se hibrida con los mRNA objetivo para poder generar su silenciamiento.
Estructura de DICER1
- El gen humano DICER1 está ubicado en el cromosoma 14q32.13 y está compuesto por 27 exones con 1,922 aminoácidos. La proteína DICER1 es una enzima grande de multidominio con forma de “L”.
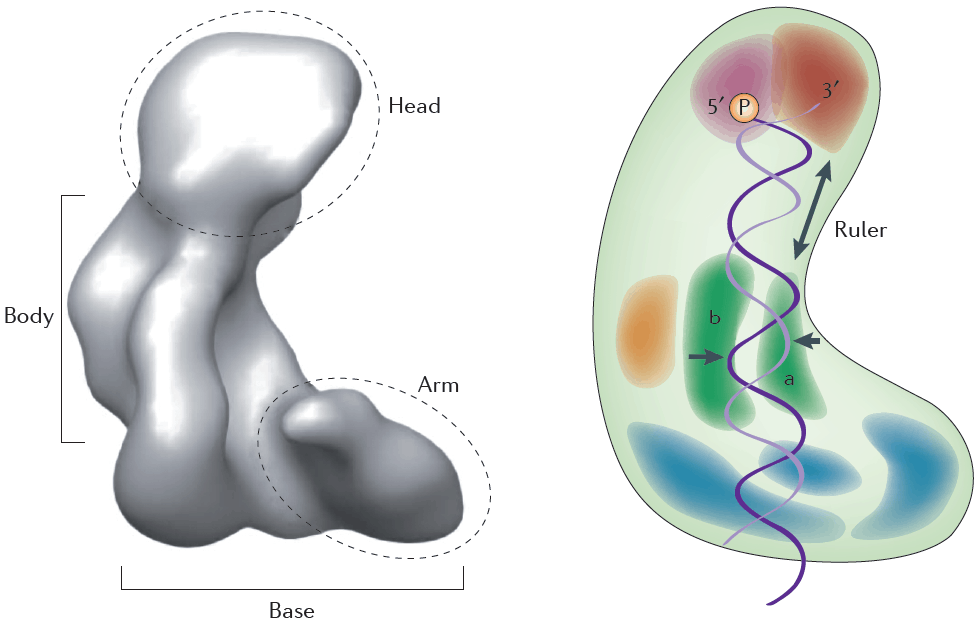
- En la parte superior de la “L” se encuentran los dominios PAZ y Plataforma. Estos dominios son las zonas de enlace para el RNA de doble cadena (dsRNA). La saliente de 3’ del sustrato de dsRNA se une en el dominio PAZ y la saliente de 5’ se une en el dominio Plataforma.
- La parte inferior del DICER1 consta de dominios RNase IIIa y RNase IIIb, que se dimerizan para formar el núcleo catalítico fundamental de la enzima y cada uno adhiere una cadena del sustrato de dsRNA. El dominio RNase IIIa es el responsable de producir 3p miRNA a partir de la cadena 3’ y el dominio RNase IIIb produce 5p miRNA a partir de la cadena 5’. DICER1 requiere iones de magnesio o de manganeso para poder llevar a cabo el clivaje catalítico. Estos iones de metal están unidos a residuos de unión de iones dentro de los dominios RNase III en los residuos de aminoácidos E1320 y E1564 en el dominio RNase IIIa, y D1709 y E1813 en el dominio RNase IIIb.
- Correlación clínica: La mayoría de las personas con tumores relacionados con el síndrome de DICER1 albergan dos mutaciones en DICER1. Generalmente estas consisten de una mutación (inactivante) truncada de línea germinal heterocigótica, que puede estar ubicada en cualquier posición en todo el gen, acoplado a una mutación sin sentido somática (o específica de un tumor), que afecta consistentemente a uno de los residuos de unión de iones de metal dentro del dominio RNase IIIb o un residuo adyacente. Se ha descubierto que casi todos los tumores y displasias asociados al síndrome albergan dichas mutaciones de “zonas de riesgo”. En un subgrupo muy pequeño de pacientes con síndrome de DICER1, los eventos mutacionales iniciales son mutaciones de RNase IIIb en mosaico; el fenotipo en estos casos puede ser más severo.
- Los dominios RNase III están separados de los dominios de unión de dsRNA por un ligador, que contiene una hélice conectora. Esto mantiene el esqueleto de fosfato de dsRNA en su lugar. También actúa como una “regla” al posicionar al pre-miRNA a lo largo de la enzima para que la enzima pueda adherir el dsRNA a los miRNA de los tamaños apropiados.
- En la base de la L se encuentra el dominio DExD/H box helicasa. Se cree que este dominio se sujeta al sustrato dsRNA.
Características/fenotipo clínico
En 2009, las mutaciones DICER1 de línea germinal heterocigótica se identificaron en 11 familias con una o dos personas con blastoma pleuropulmonar (PPB) e historiales familiares con otros varios tumores. Al hacerlo, se describió un nuevo síndrome de predisposición cancerígena hereditaria, llamado “síndrome de DICER1” por Slade y otros (OMIM #601200).
Desde ese momento, el espectro fenotípico se expandió a través de la identificación de varias otras familias con mutaciones DICER1 de línea germinal, que incluyen familias con y sin PPB, para incluir la predisposición a tumores adicionales, que incluyen notablemente el nefroma quístico (CN), los tumores estromales del cordón sexual ovárico (OSCST, especialmente los tumores de células de Sertoli-Leydig (SLCT)), el bocio multinodular (MNG), el rabdomiosarcoma embrionario de cérvix (cERMS) y el blastoma pituitario (PitB), entre otros. No es inusual la participación bilateral de órganos en órganos pareados. Se describen las mutaciones de línea germinal de DICER1 en personas con otros varios tipos de tumores y se están agregando nuevos tumores al espectro del síndrome DICER1. Consulte la pestaña “Fenotipos” para obtener más información sobre los tumores asociados al síndrome de DICER1.
Muchos de los tumores observados en el síndrome de DICER1 son bastante raros o inusuales. Se sugiere la prueba genética de la línea germinal y el asesoramiento genético para el paciente o su familia en caso de alguna de las siguientes circunstancias: (a) un diagnóstico de cualquiera de los tumores muy característicos (p. ej. PPB, CN, PitB); (b) una coocurrencia en un paciente o familiar de cualquiera de los tumores asociados al DICER1.
Muchos de los tumores relacionados con el DICER1 se presentan antes de los 15 a 25 años de edad e incluso algunos se presentan en la primera infancia como PPB, CN y PitB. Sin embargo, la enfermedad de tiroides y algunos tumores (como cERMS y OSCST) pueden aparecer a los 40 a 50 años de edad.
La penetrancia de las mutaciones de DICER1 con respecto al desarrollo de tumores no se conoce de manera definitiva en este momento aunque aparenta ser baja y variable, incluso dentro de las familias. Es necesario realizar más estudios para aclarar la verdadera penetrancia del síndrome de DICER1, ya que se puede presentar con fenotipos subclínicos, como quistes pulmonares o renales o nódulos tiroideos minúsculos. La penetrancia parece ser mayor en las mujeres debido a la ocurrencia de tumores ginecológicos y la enfermedad de tiroides más frecuente. Parece que, por lo menos, el 50 % de los portadores femeninos y quizás el 80 % de los portadores masculinos no se verán afectados clínicamente.
Mutaciones de DICER1: línea germinal y somática
El síndrome de DICER1 se caracteriza por las mutaciones de línea germinal heterocigótica (mutaciones en una de las dos copias del gen DICER1 de la persona en cada célula de su cuerpo) y presenta una herencia dominante autosómica. Los hijos de una persona con una mutación de línea germinal DICER1 posee un 50 % de probabilidades de heredar la mutación y, por lo tanto, estar en riesgo de contraer tumores relacionados con DICER1 y el 50 % de probabilidades de no heredar la mutación y, por lo tanto, no tener un riesgo aumentado con respecto a los tumores relacionados con DICER1. La mayoría de las mutaciones de DICER1 son heredadas de un padre que también es portador de la mutación (quien puede tener o no un historial personal de tumores relacionados con DICER1). En el 20 % de los casos, aproximadamente, las pruebas familiares revelan que la mutación de DICER1 se encuentra de novo en la persona afectada. En este caso, se presume que los hermanos de la persona afectada no están en riesgo con respecto a los tumores relacionados con DICER1. En el síndrome de DICER1, no se observó el mosaicismo gonadal, el fenómeno en el que un padre no es portador de la mutación de DICER1 de línea germinal, pero que posee una mutación de DICER1 en una subpoblación de células ubicadas específicamente en las gónadas, aunque es posible, en teoría. Por lo tanto, se podrían tener en cuenta las pruebas genéticas para los hermanos de niños con una mutación aparentemente de novo, a pesar de que sea extremadamente poco probable un resultado positivo.
Las mutaciones de línea germinal en DICER1 son generalmente truncadas (a pesar de que se observan raramente las mutaciones sin sentido patógena) y se identificaron en todo el gen. Se observaron mutaciones de DICER1 de línea germinal en varios grupos étnicos y no se observaron efectos fundadores. No hay correlaciones de genotipo-fenotipo consistentes entre las mutaciones de línea germinal y la penetrancia tumoral asociada.
El síndrome de DICER1 se adapta al modelo de un gen supresor tumoral (TSG), en el sentido en que el gen es funcionalmente inactivado por las mutaciones bialélicas (una mutación de línea germinal y una somática, en el contexto del síndrome de DICER1). Sin embargo, el DICER1 difiere de la mayoría de los otros TSG en que la segunda mutación o el “segundo golpe”, observado en los tumores relacionados con DICER1 se encuentra casi siempre limitado al dominio de RNase IIIb. Estos segundos golpes somáticos son posiciones muy características, que afectan los aminoácidos 1705, 1709, 1809, 1810 y 1813 que alteran aunque no destruyen la función DICER1. Estas “zonas de riesgo” son residuos de unión de metales, que son importantes para la función enzimática, o que permanecen adyacentes a estos residuos. Las mutaciones de estas posiciones de aminoácidos llevan a la pérdida de una síntesis de 5p microRNA. No es frecuente la pérdida de heterocigosidad (LOH) en los tumores relacionados con DICER1 como un evento somático secundario, aunque ocurre ocasionalmente, en especial en el caso del pineoblastoma.
Se observó el mosaicismo somático de las mutaciones de las zonas de riesgo en el dominio RNase IIIb en niños con fenotipos severos notables para los tumores primarios múltiples y, en algunos casos, un sobrecrecimiento. Estas mutaciones parecen estar acompañadas de mutaciones truncadas somáticas en el otro alelo o LOH en los tumores.
Espectro del tumor del síndrome de DICER1
El PPB es un tumor raro que surge durante el desarrollo pulmonar fetal e infantil. Se cree que es la manifestación potencialmente mortal más común del síndrome de DICER1. Desde el nacimiento hasta aproximadamente los 2 años, el PPB generalmente se presenta como una masa quística (PPB Tipo I). Desde aproximadamente los 2 a 6 años, el PPB puede presentarse como una combinación de quistes pulmonares y un tumor sólido (PPB Tipo II) o como un tumor completamente sólido (PPB Tipo III). Los PPB Tipos II y III son tumores altamente malignos con tasas de curación que son mucho más bajas que en el PPB Tipo I. El PPB Tipo I puede avanzar hasta los Tipos II y Tipos III, enfatizando la importancia de la detección y resección temprana. Los niños con PPB pueden presentar dificultad para respirar o neumotórax debido a la ruptura quística. En casos de una enfermedad avanzada, pueden presentar además pérdida de peso y fiebre. PMID: 8636815, 25209242, 19556464.
El CN generalmente se considera una displasia renal benigna, que consta de varios quistes multiloculares de pared fina. Es una de las manifestaciones más frecuentes del síndrome de DICER1, que generalmente ocurre antes de los 4 años en portadores de la mutación, la cual se presenta como una masa abdominal o lateral indolora. Mientras sea no neoplástica, se puede requerir una nefrectomía parcial o total debido al efecto de masa o a causa de una deficiencia de la función renal. En casos muy raros, se observó que el CN evolucionó hasta convertirse en un sarcoma anaplásico de riñón, un neoplasma maligno. PMID: 21036787, 17137906, 24481001, 28177962
El MNG se caracteriza por el agrandamiento nodular de la glándula tiroides. El MNG es la manifestación más frecuente del síndrome de DICER1 y se presenta como una masa palpable en el cuello, generalmente desde la niñez hasta principios de la edad adulta. El MNG y la enfermedad de tiroides son comunes en la población general y, por lo tanto, se debería considerar al síndrome de DICER1 para el MNG solamente en presencia de los tumores relacionados con DICER1 adicionales en la persona o la familia. El DTC es una manifestación rara del síndrome de DICER1 y se lo observó en niños que recibieron un tratamiento fuerte (quimioterapia, radioterapia) por un diagnóstico previo de PPB al igual que en aquellos sin factores de riesgo previos para el cáncer de tiroides. PMID: 21205968, 24617712.
Los OSCST son un grupo de cánceres ováricos no epiteliales poco frecuentes e incluyen tumores de células de la granulosa y tumores de células de Sertoli-Leydig (SLCT). El SLCT es el OSCST más comúnmente observado en el síndrome de DICER1. A pesar de que el SLCT es un tumor maligno, la mortalidad asociada es baja. El SLCT se presenta frecuentemente con signos de virilización (hirsutismo, cambios de voz), junto con las características típicas de un neoplasma ovárico, que incluye la distensión y el dolor abdominal.. PMID: 21205968, 21501861, 25844550, 27858560.
El PitB es un tumor primitivo extremadamente raro de la glándula pituitaria que generalmente se presenta antes de los 24 meses, a menudo con el síndrome de Cushings o con oftalmoplejia o hidrocefalia. El PitB es un tumor potencialmente mortal. Es una manifestación muy rara aunque altamente característica del síndrome de DICER1. PMID: 24839956.
El PinB es un tumor neuroectodérmico primitivo de la glándula pineal. Presenta características que incluyen síntomas de cambios oftalmológicos y de masa pineal o pituitaria. El PinB es una manifestación rara aunque característica del síndrome de DICER1. Tiende a ocurrir a una edad más temprana si está presente la mutación de DICER1 de línea germinal. PMID: 25022261.
El cERMS es un tumor embrionario raro que generalmente se diagnostica en la niñez y la adolescencia. Presenta características que incluyen un manchado o sangrado anormal y una masa polipoide vaginal. Se observaron otros rabdomiosarcomas embrionarios en el síndrome de DICER1, como en la vejiga y el ovario PMID: 22180160.
El NCMH es un tumor benigno muy raro de las cavidades nasales y el seno, que a menudo se presenta con congestión nasal en la niñez o adolescencia. El NCMH es una manifestación rara aunque de algún modo característica del síndrome de DICER1. PMID: 25118636.
En las personas con mutaciones de DICER1 en línea germinal pueden ocurrir otros tumores/displasias como tumores de Wilms, neuroblastomas, meduloblastomas, pólipos hamartomatosos intestinales juveniles, hamartoma mesenquimatoso hepático y quistes hepáticos y sarcomas paratesticulares atípicos. La gran mayoría de los casos no están causados por mutaciones en DICER1 y la observación de alguna de estas características de manera aislada en un paciente no es suficiente para sugerir el síndrome de DICER1. Sin embargo, el riesgo a desarrollar estas lesiones parece estar aumentado en los portadores de mutación en DICER1 y se puede recomendar realizar la prueba genética para detectar mutaciones en DICER1 si estas lesiones ocurren en el contexto de familias o individuos que han desarrollado tumores típicamente asociados con DICER1. Recientemente, se han encontrado mutaciones en DICER1 en cuatro teratomas malignos de glándula tiroidea y dos tumores teratoides malignos en región presacra. La presencia de una variante patogénica en DICER1 en línea germinal confirmó el síndrome de DICER1 en uno de los pacientes con teratoma en región presacra; en el resto de casos, sólo se evaluaron las mutaciones somáticas. PMID: 23620094, 28766837, 25190313, 31067372, 32222066, 31917706, 31296931.
Adaptada de Foulkes WD, Priest JR, Duchaine TF. DICER1: mutations, microRNAs and mechanisms. Nat Rev Cancer. 14 de ocutbre de 2014 (10):662-72. doi: 10.1038/nrc3802. Epub 2014 Sep 1.
| wdt_ID | Phenotype and Relative Frequency | Notation | Does this disease by itself suggests DICER1 Mutation Testing? | Approximate Ages of Susceptibility, range (peak). | Malignant or Benign | Deaths recorded in cases with DICER1 syndrome |
|---|---|---|---|---|---|---|
| 3 | Most Frequent Phenotypes | |||||
| 4 | pleuropulmonary blastoma | PPB | yes | |||
| 5 | Type I (cystic) PPB | 0 - 24 m (8 m ) | M | y, if progresses to Type II or III | ||
| 6 | Type II (cystic/solid) PPB | 12 - 60 m (31 m) | M | y, ~40% | ||
| 7 | Type III (solid) PPB | 18 - 72 m (44 m) | M | y, ~60% | ||
| 9 | Type Ir (cystic) PPB | any age | B or M | none observed | ||
| 10 | multinodular goiter | MNG | no | 5 - 40 y (10 - 20 y) | B | n |
| 11 | cystic nephroma | CN | yes | 0 - 48 m (undetermined) | B | n (see anaplastic sarcoma of kidney below) |
| 12 | Sertoli-Leydig cell tumor of ovary | SLCT | yes | 2 - 45 y (10 - 25 y) | M | y, < 5% of cases |
| 13 | Moderate Frequency Phenotypes |
Detección
La identificación de las mutaciones de línea germinal del DICER1 en pacientes y sus familiares es importante para evaluar el riesgo futuro de neoplasia y permite la oportunidad de realizar pruebas predictivas para las familias para identificar las personas en riesgo con respecto a los tumores relacionados con DICER1.
Debido a la naturaleza única y rara de muchos de los tumores relacionados con DICER1 conocidos, la presencia de alguno de los tipos de tumores distintivos por sí solos (PPB, CN, SLCT, cERMS, PitB, PinB, NCMH y CBME) ameritaría que se realice una derivación al servicio de genética del cáncer para obtener asesoramiento y una prueba genética de línea germinal del gen DICER1. De la misma manera, las historias familiares que contribuyen a la presencia de características relacionadas con DICER1 menos distintivas, como un MNG de aparición temprana o los tumores de Wilms, pueden ameritar una derivación a genética si tienen lugar en familias con tumores relacionados con DICER1 en familiares cercanos. Varios casos de MNG en una familia pueden ser suficiente para considerar realizar una derivación a un servicio de genética.
La identificación de una mutación de DICER1 de línea germinal permite que las personas reciban un seguimiento médico personalizado y que consideren la evaluación de los tumores relacionados con DICER1. La vigilancia del tumor permite la identificación de un tumor en una etapa temprana, por lo que puede ser removido y tratado con las menores consecuencias posibles. Específicamente, evaluar a los recién nacidos que portan la mutación con respecto a un PPB Tipo I quístico temprano puede permitir una remoción quirúrgica y evitar que la enfermedad avance al PPB Tipo II o III que conlleva pronósticos mucho más desfavorables. Sin embargo, muchos fenotipos de DICER1 tienden a no ser potencialmente mortales y ocurrir a lo largo de un rango etario amplio. Por lo tanto, se deben sopesar cuidadosamente los rituales de evaluación de varios años en comparación con la morbidez potencial de dichos programas.
Se puede evaluar a los familiares no afectados de una persona con una mutación de DICER1 de línea germinal con respecto a la mutación de DICER1 familiar para confirmar o descartar el estado de riesgo. Debido a que la penetrancia del síndrome de DICER1 con respecto a los tumores parece ser bastante baja, la evaluación genética en cascada de los familiares puede identificar la mutación de DICER1 familiar en parientes no afectados que pueden tener riesgo de tumores o pueden beneficiarse a partir del conocimiento de una intervención temprana, como una prueba y evaluación genética de tumores en infantes.
Vigilancia
No existen pautas establecidas para la vigilancia del tumor en los portadores de la mutación de DICER1.
Las siguientes estrategias de evaluación fueron sugeridas por el taller de predisposición al cáncer en la niñez AACR (Schultz KAP et al, PTEN, DICER1, FH and their associated tumor susceptibility syndromes: Clinical features, genetics and surveillance recommendations in childhood. Clin Cancer Res 2017 15;23(12):e76-e82). Las instituciones específicas pueden tener recomendaciones diferentes. Es importante reconocer que la mayoría de los datos se basan solamente en la opinión experta.
Órgano | Tipos de tumores observados | Presentación de los síntomas | Vigilancia en portadores de mutación conocidos |
Pulmones | PPB Tipos I, II, II, Ir | Dificultad respiratoria, dolor de pecho, fiebre y pérdida de peso | – CT de pecho inicial entre los 3 y 6 meses de edad. – Si es normal, CT de pecho entre los 2.5 y 3 años de edad. – Se debe considerar una radiografía de pecho cada 6 meses hasta los 8 años de edad y luego una vez por año de los 8 a los 12 años de edad. |
Riñones | CN, ASK, WT | Masa abdominal, dolor, sangre en la orina
| – Considerar un ultrasonido abdominal cada 6 meses hasta los 8 años de edad. – Anualmente de ahí en adelante hasta los 12 años de edad dependiendo de los hallazgos. |
Cerebro | PinB, PitB | Pineoblastoma: síntomas de la masa pineal o pituitaria, cambios oftalmológicos. Blastoma pituitario: Síndrome de Cushings, oftalmoplejia o diabetes insípida. | – Se puede considerar la MRI cerebral de control, aunque es controvertida, ya que la relación riesgo/beneficio todavía no es conocida y estos tumores son los dos manifestaciones raras del síndrome de DICER1 (<1%). – MRI cerebral urgente si se presenta alguno de los síntomas de una patología intracraneana. |
Ginecológica | OSCST (SLCT, ginandroblastoma), cERMS, oERMS | OSCST: masa/distensión abdominal, irregularidades menstruales, signos de virilización. cERMS: manchado vaginal, masa polipoide que se extiende desde la vagina. | – Considerar un ultrasonido pélvico anual o semestral (al mismo tiempo que una vigilancia renal) cada 6 a 12 meses desde el nacimiento hasta la adultez. |
Tiroides | Nódulos tiroideos, MNG, cáncer de tiroides diferenciado | Nódulos palpables, síntomas de compresión locales (disfagia, disfonía, estridor) | – Considerar ultrasonido de la tiroides con una evaluación de una adenopatía local a los 8 años de edad. – Si fuera normal, repetir cada 3 años. |
Ojos | CBME | Aspecto inusual con respecto a la pupila, deficiencia en la visión | – Conciencia del riesgo. |
Nariz | NCMH | Congestión nasal o “congestión” | – Conciencia del riesgo. – ENT con endoscopía nasal si estuvieran presentes los síntomas de una obstrucción nasal. |
GI | Pólipos hamartomatosos | Obstrucción intestinal: hinchazón, dolor | – Conciencia del riesgo. – Evaluación si están presentes los síntomas de una obstrucción intestinal. |
* Estas recomendaciones pueden cambiar a medida de que haya más información disponible con respecto al espectro de los tumores en el síndrome de DICER1.
Tratamiento
No existe evidencia para sugerir que los tumores asociados a las mutaciones de DICER1 de línea germinal poseen resultados de tratamientos diferentes que si los mismos tumores ocurrieran esporádicamente.
La mayoría de los tumores en el espectro del síndrome de DICER1 poseen un curso relativamente benigno. Sin embargo, la neoplasia tiene lugar en ciertos tipos de tumores relacionados con el DICER1, notablemente en el PPB. Otros están asociados a la morbidez o la mortalidad debido a la ubicación y efectos del crecimiento, como el PitB o las manifestaciones clínicas como la androgenización debido al SLCT. Debido a que el síndrome de DICER1 es raro, los médicos que encuentran enfermedades relacionadas con el DICER1 deberían considerar comunicarse con expertos en el síndrome para obtener las recomendaciones sobre el tratamiento más recientes.

