Esta seção é uma adaptação do artigo: “DICER1: mutações, microRNAs e mecanismos”, publicado na Nature Reviews Cancer por Foulkes, Priest and Duchaine (PMID 25176334). Para mais informações, consulte o artigo original.
Para obter uma lista atualizada de artigos publicados sobre o gene DICER1 e a síndrome DICER1, clique aqui.
Funções Moleculares
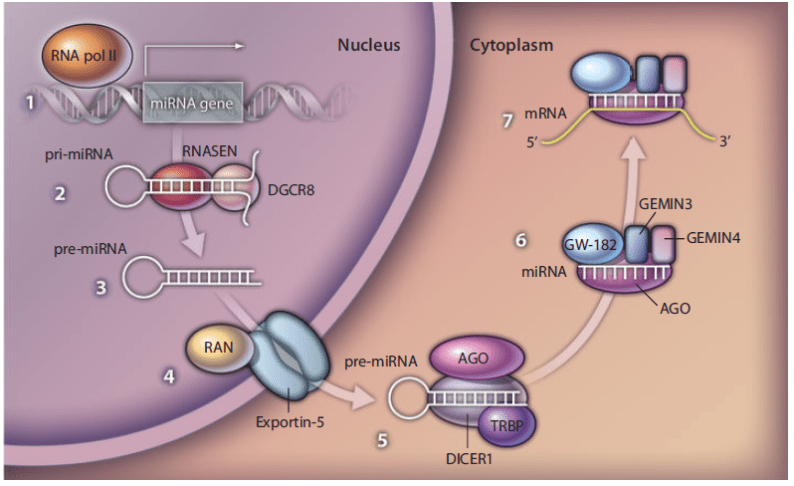
A proteína Dicer é uma endoribonuclease responsável pela produção de microRNAs maduros (miRNAs), que são pequenas moléculas de RNA de fita simples que têm como alvo RNAs mensageiros (mRNAs) e têm um papel importante na regulação da expressão gênica por reprimir a síntese proteica. A forma humana da proteína Dicer é chamada DICER1, codificada pelo gene DICER1, e é amplamente expressa nos tecidos. O DICER1 está envolvido na via de silenciamento gênico mediada por miRNA, onde um miRNA hibridiza imperfeitamente com mRNAs-alvo. Essa hibridização, por sua vez, geralmente leva à repressão da tradução do mRNA e ao início da redução de expressão do mRNA. Um transcrito primário de miRNA (pri-miRNA) é produzido via transcrição de um gene de miRNA pela enzima RNA polimerase II. O pri-miRNA é então processado no núcleo por DROSHA (também conhecido como RNASEN), uma endonuclease de RNA e a proteína de ligação a RNA DGCR8 (também conhecida como PASHA), resultando na produção de um stemloop de RNA que contém o miRNA. Essa estrutura (hairpin ) inicial de miRNA (pre-miRNA) é subsequentemente exportado para o citoplasma através de poros nucleares. A proteína DICER1 citoplasmática então cliva o pré-miRNA para liberar o miRNA curto (~ 21 nucleotídeo) maduro. Este miRNA é então carregado por uma proteína Argonaute (AGO) formando o núcleo do complexo silenciador induzido por miRNA (miRISC). O miRISC hibrida então com mRNAs direcionados para gerar seu silenciamento gênico.
Estrutura de DICER1
O gene DICER1 está localizado no cromossomo 14q32.13 e é composto por 27 exons com 1.922 aminoácidos. A proteína DICER1 é uma grande enzima com vários domínios e em formato de “L”.
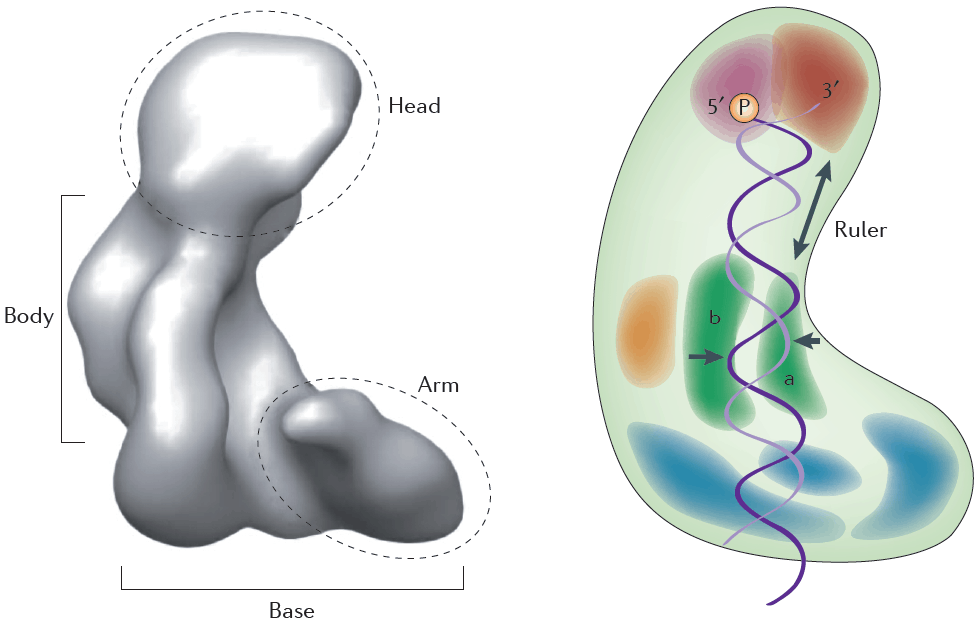
- No topo do “L” estão os domínios PAZ e Platforma. Estes domínios são bolsas de ligação para RNA de cadeia dupla (dsRNA). A protuberância 3 ‘do substrato de dsRNA liga-se ao domínio PAZ e a porção 5’ se liga ao domínio Plataforma
- A metade inferior de DICER1 consiste nos domínios RNase IIIa e RNase IIIb, que dimerizam para formar o núcleo catalítico crítico da enzima, sendo que cada um cliva uma cadeia do substrato de dsRNA. O domínio RNase IIIa é responsável pela produção de 3p miRNAs da cadeia 3 ‘, e o domínio RNase IIIb produz 5p miRNAs da cadeia 5’. O DICER1 requer íons de magnésio e / ou manganês para realizar a clivagem catalítica. Estes íons metálicos estão ligados a resíduos de ligação a íons dentro dos domínios da RNase III nos resíduos de aminoácidos E1320 e E1564 no domínio da RNase IIIa, e D1709 e E1813 no domínio da RNase IIIb.
- Correlação clínica: A maioria dos indivíduos com tumores relacionados com a síndrome DICER1 apresenta duas mutações no DICER1. Estes consistem tipicamente de uma mutação heterozigótica truncada (inativadora) germinativa, que pode estar localizada em qualquer posição em todo o gene, acoplada a uma mutação somática (ou específica do tumor), que afeta consistentemente um dos sítios de ligação de íons metálicos dentro do domínio de RNase IIIb ou um resíduo adjacente. Quase todos os tumores e displasias associados com a síndrome apresentam tais mutações “hotspot”. Em um subgrupo muito pequeno de pacientes com a síndrome DICER1, os eventos mutacionais iniciais são mutações da RNase IIIb em mosaico; o fenótipo nestes casos pode ser mais grave.
- Os domínios da RNase III são separados dos domínios de ligação do dsRNA por um ligante, que contém uma hélice conectora. Isso mantém o backbone de fosfato de dsRNA no lugar. Ele também atua como uma “régua”, posicionando o pré-miRNA ao longo da enzima de forma que a enzima possa clivar o dsRNA em miRNAs de tamanhos apropriados.
- Na base do L está o domínio helicase \ DExD / H. Este domínio é considerado um repressor do substrato de dsRNA.
Características Clínicas / Fenótipo
Em 2009, foram identificadas mutações germinativas DICER1 heterozigóticas em 11 famílias com um ou mais indivíduos com blastoma pleuropulmonar (PPB) e histórias familiares de vários outros tumores. A partir destes achados, uma nova síndrome hereditária de predisposição ao câncer foi descrita, intitulada por Slade et al como “síndrome DICER1” (OMIM # 601200).
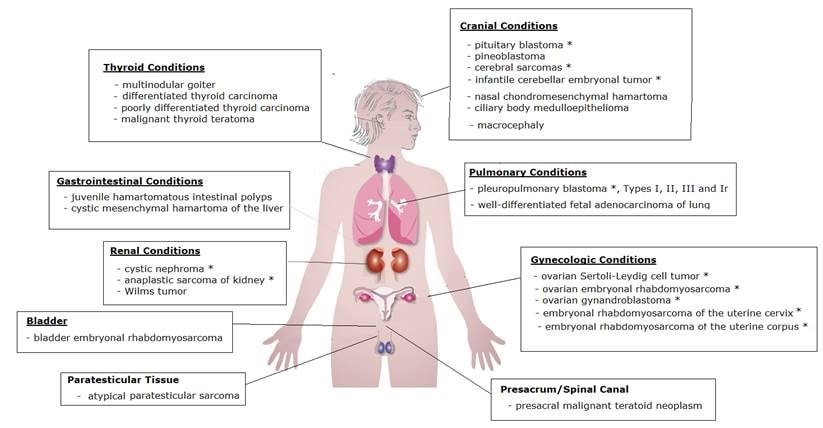
Desde então, o espectro fenotípico da Síndrome DICER1 foi expandido através da identificação de muitas outras famílias com mutações DICER1 germinativas, com e sem PPB,. Foram incluídos predisposição para outros tumores, notadamente o nefroma cístico (NC), tumores estromais do cordão sexual do ovário (OSCSTs, especialmente Tumores de células de Sertoli-Leydig (SLCT)), bócio multinodular (MNG), rabdomiossarcoma embrionário cervical (cERMS) e blastoma hipofisário (PitB), entre outros. O envolvimento bilateral não é incomum em órgãos pareados. Mutações germinativas de DICER1 foram descritas em indivíduos com vários outros tipos de tumores, e novos tumores ainda estão sendo adicionados ao espectro da síndrome DICER1. Consulte a guia “Fenótipos” para obter mais informações sobre os tumores associados à síndrome DICER1.
Muitos dos tumores observados na síndrome DICER1 são bastante raros ou incomuns. O teste genético para pesquisa de mutação germinativa para DICER1 e o aconselhamento genético para um doente e / ou família poderão ser sugeridos para qualquer uma das circunstâncias que se seguem: (a) diagnóstico de um dos tumor altamente característicos para a síndrome (por exemplo, PPB, CN, PitB); (b) uma co-ocorrência em um paciente ou família de qualquer um dos tumores associados ao DICER1.
Muitos dos tumores relacionados a síndrome DICER1 apresentam-se antes dos 15 a 25 anos de idade, com alguns ocorrendo muito precocemente na infância, como PPB, CN e PitB. No entanto, doenças da tireoide e alguns outros subtipos de tumores (como cERMS e OSCST) podem aparecer até os 40 a 50 anos de vida.
A penetrância para o desenvolvimento de tumores em portadores de mutações germinativas de DICER1 não é completamente conhecida neste momento, mas parece ser baixa e variável, mesmo dentro das famílias afetadas. Mais estudos são necessários para esclarecer a verdadeira penetrância da síndrome DICER1, pois ela pode se apresentar com fenótipos subclínicos como cistos pulmonares ou renais, ou nódulos de tireoide muito pequenos. A penetrância parece ser maior no sexo feminino devido à ocorrência de tumores ginecológicos e doenças da tireoide com maior frequencia. Estima-se que pelo menos 50% dos portadores do sexo feminino e ao redor de 80% dos portadores do sexo masculino permanecerão clinicamente não afetados por tumores.
Mutações em DICER1 – Germinativas e Somáticas
A síndrome DICER1 é caracterizada por mutações germinativas heterozigóticas (mutações em uma das duas cópias do gene DICER1 de um indivíduo em cada célula do corpo) e exibe herança autossômica dominante. Crianças de um dos pais com uma mutação germinativa em DICER1 têm 50% de chance de herdar a mutação e, portanto, estar em risco para desenvolver os tumores relacionados ao DICER1; 50% não herdam a mutação e, portanto, não estarão sob risco aumentado para o desenvolvimento de tumores relacionados a síndrome DICER1. A maioria das mutações em DICER1 é herdada de um pai que também carrega a mutação (que pode ou não ter um histórico pessoal de tumores relacionados ao DICER1). Em cerca de 20% dos casos, o teste familiar revela que a mutação DICER1 é de novo (ocorreu pela primeira vez) no indivíduo afetado. Neste caso, os irmãos do indivíduo afetado provavelmente não estarão sob sob risco para o desenvolvimento de tumores relacionados ao DICER1. O mosaicismo gonadal, fenômeno no qual um genitor não carrega uma mutação DICER1 germinativa, mas tem uma mutação DICER1 em uma subpopulação de células especificamente localizadas nas gônadas, não foi observado na síndrome DICER1, mas é teoricamente possível. Portanto, testes genéticos poderiam ser considerados para irmãos de crianças com uma mutação aparentemente de novo, embora um resultado positivo seja extremamente improvável.
As mutações germinais no gene DICER1 são tipicamente truncadas (embora mutações do tipo missense e patogênicas tenham sido raramente observadas) e foram identificadas em todo o gene. Mutações germinativas em DICER1 foram observadas em muitos grupos étnicos, e não foram observados efeitos fundadores. Não existem correlações genótipo-fenótipo consistentes entre as mutações germinativas e a penetrância tumoral associada.
A síndrome de DICER1 se encaixa no modelo de um gene supressor de tumor (GST), em que o gene é funcionalmente inativado por mutações bialélicas (uma ocorrendo de forma germinativa e uma segunda mutação somática, no contexto da síndrome DICER1). No entanto, a síndrome DICER1 difere da maioria dos outros GSTs em que a segunda mutação, ou “segundo hit“, observado nos tumores relacionados com DICER1 é quase sempre limitada ao domínio RNase IIIb. Estes segundos eventos somáticos são altamente característicos, afetando as posições de aminoácidos 1705, 1709, 1809, 1810 e 1813 que alteram mas não destroem o DICER1. Estes “hotspots” são resíduos de ligação a metais, que são importantes para a função da enzima, ou estão adjacentes a estes resíduos. Mutações nessas posições de aminoácidos levam à perda da síntese de microRNA 5p. A perda de heterozigosidade (LOH) é incomum nos tumores relacionados ao DICER1 como sendo um segundo evento somático, mas ocorre ocasionalmente, especialmente no caso do pinoblastoma.
O mosaicismo somático para mutações do tipo hotspot no domínio da RNase IIIb foi relatado em crianças com fenótipos graves, caracterizados por múltiplos tumores primários e, em alguns casos, crescimento excessivo. Estas mutações parecem ser acompanhadas por mutações somáticas truncadas no outro alelo ou LOH nos tumores.
Espectro de Tumores Associados a DICER1
O BPP é um tumor raro que surge durante o desenvolvimento pulmonar fetal e infantil. Acredita-se que seja a manifestação mais comum relacionada a risco de morte na síndrome DICER1. Desde o nascimento até aproximadamente 2 anos de idade, o PPB apresenta-se tipicamente como uma massa cística (BPP Tipo I). De aproximadamente 2 a 6 anos de idade, o BPP pode apresentar-se como uma combinação de cistos pulmonares e tumor sólido (BPP Tipo II), ou como tumor puramente sólido (BPP Tipo III ). Tipos II e III do BPP são tumores altamente malignos com taxas de cura muito inferiores às do BPP tipo I. O BPP tipo I é capaz de progredir para os tipos II e III, enfatizando a importância da detecção e ressecção precoces. Crianças com BPP podem apresentar falta de ar e pneumotórax devido à ruptura do cisto. Em casos de doença avançada, eles também podem apresentar perda de peso e febre. PMID: 8636815, 25209242, 19556464.
O NF é geralmente considerado uma displasia renal benigna, constituído por múltiplos cistos renais multiloculares de paredes finas. É uma das manifestações mais frequentes da síndrome DICER1, ocorrendo tipicamente abaixo dos 4 anos de idade em portadores de mutação, apresentando-se como uma massa indolor abdominal ou no flanco. A nefrectomia parcial ou total pode ser necessária devido a um efeito de massa ou devido ao comprometimento da função renal. Em casos muito raros, observa-se que o NC evolui para sarcoma anaplásico do rim, uma neoplasia maligna. PMID: 21036787, 17137906, 24481001, 28177962
O BMN é caracterizado pelo aumento nodular da glândula tireóide. O BMN é a manifestação mais frequente da síndrome DICER1 e se apresenta como uma massa cervical palpável, tipicamente desde a infância até o início da idade adulta. O BMN e a doença da tireóide são comuns na população geral e, portanto, a síndrome DICER1 deve ser considerada para o BMN somente na presença de tumores relacionados a síndrome DICER1 no indivíduo ou na família. O câncer diferenciado de tireoide é uma manifestação rara da síndrome DICER1 e tem sido observado em crianças que foram tratadas intensamente (quimioterapia, radioterapia) para um diagnóstico prévio de BPP, bem como naquelas sem fatores de risco prévios para câncer de tireoide. PMID: PMID: 21205968, 24617712, 27459524.
As NCS/EO são um grupo de cânceres de ovário não-epiteliais bastante raros, e incluem tumores de células da granulosa, ginandroblastomas e tumores de células de Sertoli-Leydig (SLCT). O SLCT é o NCS/EO mais comumente observado na síndrome DICER1. Enquanto o SLCT é um tumor maligno, a mortalidade associada é baixa. A SLCT frequentemente apresenta sinais de virilização (hirsutismo, alterações na voz), juntamente com características típicas de uma neoplasia de ovário, incluindo distensão abdominal e dor. PMID: 21205968, 21501861, 25844550, 27858560.
O BH é um tumor primitivo extremamente raro da glândula pituitária, apresentando-se tipicamente aos 24 meses de idade, geralmente com síndrome de Cushing, ou com oftalmoplegia e / ou hidrocefalia. O BH é um tumor com risco de vida. É uma manifestação muito rara, mas altamente característica da síndrome DICER1. PMID: 24839956.
PMID: 24839956.
PinB é um tumor neuroectodérmico primitivo raro originário da glândula pineal. A apresentação clínica característica incluem sintomas de massa na rreunião da pineal e alterações oftalmológicas. O PinB é uma manifestação rara, mas característica da síndrome DICER1. Este tumor tende a ocorrer em idades mais jovens se uma mutação germinativa de DICER1 estiver presente. PMID: 25022261.
PMID: 25022261.
O ERMS é um achado patológico frequente em tumores relacionados à mutação DICER1. É o subtipo sarcomatoso mais prevalente dos sarcomas de padrão misto do blastoma peluropulmonar. Os ERMS de alguns locais anatômicos específicos são altamente característicos da síndrome DICER1:
O ERMS do colo uterino (cERMS), também conhecido como “EMRS botrióide do cervix uterino” é muito raro, mas parece ser altamente característico da mutação DICER1. O cERMS ocorre tipicamente nas idades entre 10 e 25 anos, apresentando-se como manchas anormais ou massa vaginal polipóide. PMID: 22180160, 24151152, 22157934, 27896549.
O ERMS ovariano (oERMS) são muito raramente observados e parece ser bastante característico da mutação DICER1. (É possível que o oERMS não seja uma entidade separada, mas sim uma subcategoria de SLCT ovariana na qual o ERMS predomina entre os elementos heterólogos encontrados nos SLCTs relacionados a síndrome de DICER1). PMID: 25844550, 25836323.
O ERMS primário de bexiga está entre os locais mais comuns do ERMS em crianças pequenas, sendo que a maioria dos casos não está relacionada com a mutação DICER1. Existem entretanto vários relatos de casos, com ou sem mutações DICER1 germinativas, que sugerem que o ERMS da bexiga é parte da síndrome DICER1, mas nenhum caso com mutações somáticas de “segundo hit” no DICER1 foi descrito em literatura. PMID: 22180160, 18000857, 20981696.
O ERMS primário de vagina / vulva e o ERMS de órbita (todos locais característicos do ERMS na primeira infância) não foram observados associados a síndrome DICER1. Do mesmo modo, o padrão alveolar de RMS também não foi associado a mutações DICER1.
NCMH is a very rare benign tumor of the nasal cavities and sinus, often presenting with nasal congestion in childhood or adolescence. NCMH is a rare, but somewhat characteristic manifestation of DICER1 syndrome. PMID: 25118636.
Outros tumores / displasias que podem ocorrer em indivíduos com mutações germinativas do DICER1 incluem tumor de Wilms, neuroblastoma, meduloblastoma e pólipos hamatomatosos juvenis intestinais. A grande maioria dos casos não é causada por mutações DICER1, e a observação de qualquer uma dessas características sozinha em um paciente não é suficiente para sugerir a síndrome DICER1. No entanto, o risco destas condições parece estar aumentado em portadores de mutação DICER1, e o teste genético para mutações DICER1 pode ser indicado se estas neoplasias estiverem presentes no contexto de tumores relacionados com a síndrome DICER1 em outros indivíduos da família.
Adapted from Foulkes WD, Priest JR, Duchaine TF. DICER1: mutations, microRNAs and mechanisms. Nat Rev Cancer. 2014 Oct;14(10):662-72. doi: 10.1038/nrc3802. Epub 2014 Sep 1.
| wdt_ID | Fenótipo e Freqüência Relativa | Notation | Esta doença sugere por si só indica testar mutação para sindrome DICER1? | Idades aproximadas de suscetibilidade, faixa de idade (pico). | Maligno (M) ou Benigno (B) | Mortes descritas nos casos de síndrome DICER1 |
|---|---|---|---|---|---|---|
| 1 | Fenótipos mais frequentes | |||||
| 2 | Blastoma Pleuro-Pulmonar (BPP) | BPP | ||||
| 3 | BPP tipo I (cistico) | 0 - 24 m (8 m ) | M | Sim, se progredir para tipo II ou III | ||
| 4 | BPP tipo II (cistico/solid) | 12 - 60 m (31 m) | M | Sim, ~40% | ||
| 5 | BPP tipo II (solido) | 18 - 72 m (44 m) | M | Sim, ~60% | ||
| 6 | BPP tipo Ir (cistico) | qualquer idade | B or M | nenhuma descrita | ||
| 7 | Bócio multinodular | BMN | não | 5 - 40 anos (10 - 20 anos) | B | não |
| 8 | Nefroma cístico | NC | sim | 0 - 48 m (indeterminado) | B | não (veja sarcoma anaplásico do rim) |
| 9 | Tumor de ováriode células de Sertoli-Leydig | TOSL | sim | 2 - 45 anos (10 - 25 anos) | M | sim, < 5% of cases |
| 10 | Fenótipos de frequencia moderada |
Detecção
A identificação de mutações germinativas DICER1 em pacientes e seus familiares é importante para avaliar risco futuro de neoplasias, e tras a oportunidade de testes preditivos para as famílias identificarem indivíduos sob risco para o desenvolvimento de tumores relacionados a síndrome DICER1.
Devido à natureza única e rara de muitos dos tumores relacionados com DICER1, a presença de qualquer um dos tipos de tumores altamente relacionados a sindrome (BPP, NC, SLCT, cERMS, PitB, PinB, NCMH e CBME) mereceria um encaminhamento para um serviço de genética de câncer para aconselhamento e teste genético de mitações germinativas em DICER1. Além disso, uma história familiar que contribua para a presença de características relacionadas ao DICER1 menos características, a exemplo de MNG de início precoce ou tumores de Wilms, pode merecer um encaminhamento para a genética, se associados a ocorrência de tumores relacionados ao DICER1 em parentes próximos. Casos múltiplos de MNGs em uma família podem ser suficientes para considerar um encaminhamento para um serviço de genética.
A identificação de uma mutação DICER1 germinativa permite que os indivíduos afetados recebam acompanhamento médico personalizado e considerem o rastreamento para tumores relacionados a síndrome DICER1. A vigilância para tumores nesses casos permite a identificação de um tumor em um estágio inical, facilitando para que ele possa ser removido e tratado com as menores sequelas possíveis. Especificamente, o rastreio de recém-nascidos para blastoma pleuropulmonar em portadores de mutação germinativa de DICER1 pode permitir a remoção cirúrgica e a prevenção da progressão da doença para PPB do Tipo II ou III, que têm prognósticos muito mais desfavoráveis. No entanto, muitos fenótipos presentes na síndrome DICER1 tendem a não ameaçar a vida e ocorrem em uma faixa etária estendida. Assim, os protocolos de rastreioem longo praz devem ser equilibrados para favorecer a detecção precoce, em detrimento a efeitos deletérios de exposição excessiva a exames e procedimentos durante a vida.
Os familiares não afetados de um indivíduo com uma mutação germinativa de DICER1 podem ser testados para a mutação DICER1 encontrada na família, a fim de se confirmar ou descartar o status de risco. Como a penetrância da síndrome DICER1 por tumores parece ser bastante baixa, a triagem genética nos familiares pode identificar a mutação DICER1 em parentes não afetados que possam estar sob risco do desenvolvimento de tumores, ou que podem se beneficiar do conhecimento da presença da mutação para intervenção precoce, a exemplo do rastreio de tumores em lactentes portadores da mutação em DICER 1.
Vigilância
Não existem diretrizes estabelecidas para a vigilância do surgimento de tumores em portadores de mutação DICER1.
As seguintes estratégias de triagem foram sugeridas pelo workshop de predisposição para câncer infantil da AACR (Schultz KAP et al, PTEN, DICER1, FH e suas síndromes de suscetibilidade tumoral associadas: características clínicas, genética e recomendações de vigilância na infância. Clin Cancer Res 2017 15; 23 ( 12): e76-e82). As Instituições podem ter recomendações diferentes. É importante reconhecer que a maioria dos dados se baseia apenas na opinião de especialistas.
| Órgão/local anatômico | Tipos de tumor observados | sintomas | Vigilância em portadores conhecidos da mutação |
| pulmões | PPB, tipos I, II, III, Ir | Desconforto respiratório, dor torácica, febre e perda de peso | – Tomografia computadorizada inicial do tórax entre 3 e 6 meses. – Se o resultado for normal, tomografia computadorizada adicional do tórax entre 2,5 e 3 anos. – A realização de uma radiografia de tórax a cada seis meses, a partir dos 8 anos de idade e, em seguida, anualmente, de 8 a 12 anos, deve ser considerada. |
| abdome | NC, SAR, WT | Massa abdominal, dor, sangue na urina
| – Considere realizar uma ultrassonografia abdominal a cada seis meses até os 8 anos de idade. – Anualmente, até os 12 anos de idade, de acordo com os resultados. |
| cérebro | PinB, BPit | Pinoblastoma: sintomas de massa na região da pineal ou hipofisária, alterações oftalmológicas. Blastoma hipofisário: síndrome de Cushing, oftalmoplegia ou diabetes insípido. | – Uma ressonância magnética para monitoramento cerebral pode ser considerada, mas é controversa porque a relação entre risco e benefício ainda não é conhecida e esses tumores são ambas manifestações raras da síndrome DICER1 (<1%). – Ressonância magnética de urgência do cérebro na presença de sintomas de patologia intracraniana. |
| ginecológico | TCSSGO (TCSL, ginandroblastoma), RMSEC, RMSEO | TCSSGO: massa / distensão abdominal, irregularidades menstruais, sinais de virilização. RMSEC: sangramentos vaginais, massa polipóide que exterioriza na vagina. | – Considere realizar uma ultrassonografia pélvica anual ou semestral (juntamente com a monitorização renal) a cada 6 a 12 meses, do nascimento até a idade adulta. |
| tiróide | Nódulos Tireoidianos, GMN, Câncer de Tireóide Diferenciado | Nódulos palpáveis, sintomas de compressão local (disfagia, disfonia, estridor) | – Considere realizar uma ultrassonografia da tireóide com determinação da presença de adenopatias locais aos 8 anos de idade. – Se o resultado for normal, repita o exame a cada três anos. |
| olhos | MECC | Aparência incomum da pupila, distúrbio da visão | – reconhecimento de risco. |
| nariz | HNCM | Congestão nasal ou “nariz entupido” | – Reconhecimento de risco. – ORL com endoscopia nasal se sintomas de obstrução nasal estiverem presentes. |
| gastrointestinal | Pólipos Hamartomatosos | Obstrução intestinal – inchaço, dor | – Reconhecimento de risco. – Avaliação se os sintomas de obstrução intestinal estiverem presentes. |
Não há evidências que sugiram que os tumores associados às mutações germinativas do DICER1 tenham diferentes desfechos de tratamento do que os mesmos tumores quando ocorrem de forma esporadica.
A maioria dos tumores no espectro da síndrome DICER1 tem um curso relativamente benigno. No entanto, a malignidade ocorre em certos tipos de tumores relacionados ao DICER1, notadamente o blastoma peluropulmonar. Outros estão associados com morbidade e / ou mortalidade devido à localização e efeitos de massa ou crescimento, como o PitB, ou morbidades relacionadas a manifestações clínicas, como a androgenização devido a SLCTs. Como a síndrome DICER1 é rara, os médicos que se deparam com doenças relacionadas ao DICER1 devem considerar entrar em contato com especialistas na síndrome para as obter recomendações mais recentes de tratamento.